Ушул макаланын мазмунун
1 аминокислоталарды иштеп чыгуу
2. Түзүмдүк касиеттери
3. Химиялык курамы
4.Classification
5. Синтез
6. Физикехимиялык касиеттери
7. Токсификация
8. Антимикроциалдык иш
9. Реологиялык касиеттери
10. Косметика тармагындагы тиркемелер
11. Күнүмдүк косметикадагы тиркемелер
Аминокислота беттери (AAS)бир же бир нече аминокислоталар менен түзүлгөн гидрофобдук топторду бириктирүү менен түзүлгөн беттик класстар. Бул учурда аминокислоталар белок гидролиздеринен же ушул сыяктуу жаңылануучу булактардан алынган синтетикалык же алынып салынышы мүмкүн. Бул документ Аас үчүн колдо болгон синтетикалык маршруттарынын майда-чүйдөсүнө чейин жана акыркы продуктулардын физикалык касиеттерин, анын ичинде эригип, дисперсия туруктуулук, уулуу туруктуулук жана биологиялык биодрейд. Саптардын классы болуп, суроо-талаптын жогорулагандыгы боюнча, AAнин өзгөрүлмө түзүмүнө байланыштуу ААнын ар тараптары көп сандаган коммерциялык мүмкүнчүлүктөрдү сунуштайт.
Сюрфактниктер, эмульсификациялардын, эмульсирлер, коррозия ингибиторлорунда кеңири колдонулганын эске алганда, мен үчүн мунайды калыбына келтирүү жана фармацевтика, изилдөөчүлөр эч качан беттикке көңүл бурбай калышкан эмес.
Сюрфактниктер дүйнө жүзү боюнча күн сайын көп өлчөмдө керектелген эң көп химиялык продуктулар жана суу чөйрөсүнө терс таасирин тийгизди.Изилдөөлөр көрсөткөндөй, салттуу схемаларды кеңири колдонуу чөйрөсүнө терс таасирин тийгизиши мүмкүн экендигин көрсөттү.
Бүгүнкү күндө, уулануу эмес, биологиялык эместиктер жана биомиитивдүүлүк - бул керектөөчүлөрдүн пайдалыгы жана аткаруусу катары керектөөчүлөр үчүн маанилүү.
Биосурфактатташтар - бактерия, козу карындар, козу карындар сыяктуу микроорганизмдер, же сырдуу түрдө чыгарылган микроорганизмдер тарабынан синтезделген экологиялык таза тургундар.Ошондуктан, фосфолипиддер, Алкил Глексиддер жана оклин аминокислоталар сыяктуу табигый амфипилиялык структуралар үчүн молекулярдык дизайны менен да молекулалык дизайны менен да даярдоого болот.
Аминокислота беттери (AAS)адатта, жаныбарлардын же айыл чарбадан алынган чийки зат менен өндүрүлгөн кадимки сюрчтиктердин бири. Акыркы жыйырма жылдын ичинде Аас Ромубдордун роман менен болгон роман серфорациялангандыгы үчүн эмес, ААларга дегелецияланбай тургандыгын жана аларга зыян келтирбегендиктен, өзүлөрүнө зыян келтирип, зыянсыздыктардан тышкары, зыянсыздыктардан тышкары, өзүлөрүнүн зыянсыздыктарын кыдырып, азыктандырып, азыктандырып, аларды азыктандырып, зыянсыздандырат.
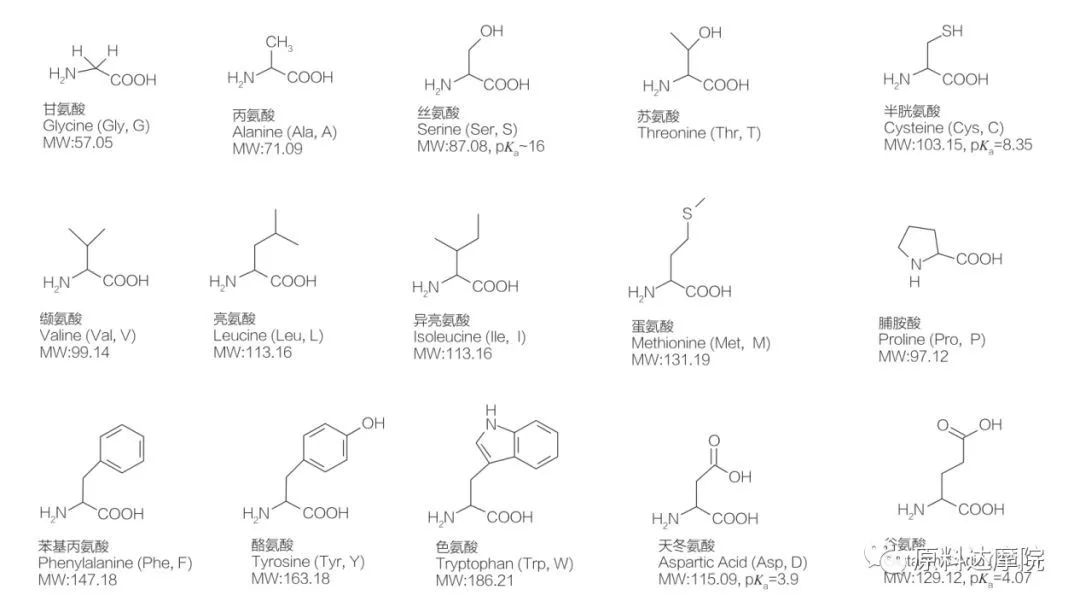
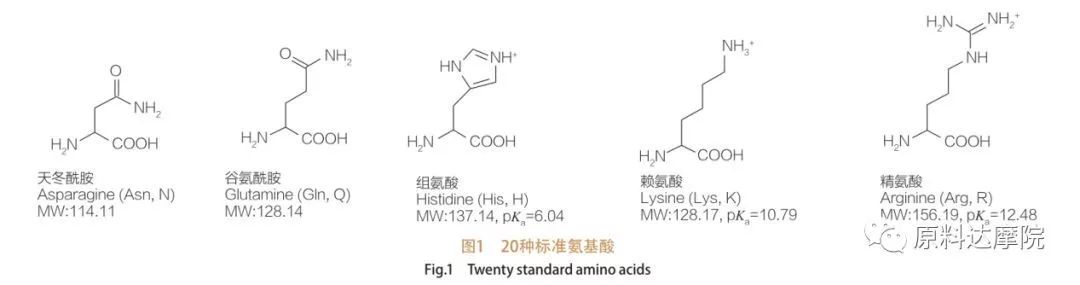
AAS аминокислоталардан турган аминокислоталардан турган аминокислоталардан турган аминокислоталардын классы катары аныкталса болот (хо 2 c-nr-nh 2) же аминокислота калдыктары (HO 2 C-CHR-NH-). Аминокислоталардын 2 функционалдык региону ар кандай сорттордун туундусуна уруксат берет. Жалпысынан 20 стандарттык протеиногендик аминокислоталар табиятта белгилүү болгон жана өсүү жана жашоо иш-аракеттериндеги бардык физиологиялык реакциялар үчүн жооптуу. R калдык r (1-сүрөт, а кгилки сайд), бул кислотанын терс лотарифми - бул кычкыл кислотасынын терс лотариифи. Айрымдары полярдык эмес жана гидрофобиялык, кээ бирлери полярдуу жана гидрофилиялык, кээ бирлери негизги жана кээ бирлери кислоталуу болушат.
Аминокислоталар кайра жаралуучу кошулмалар болуп саналат, ал эми аминокислоталардан синтезделген. Жөнөкөй жана жаратылыш түзүмү, төмөн уулуу жана тез биологиялык биологиялык курулуш көбүнчө аларды кадимки сюрфактерден жогору көтөрөт. Жаңылануучу чийки заттарды колдонуу (мисалы, аминокислоталар жана өсүмдүк майлары), AAS ар кандай биотехнологиялык маршруттар жана химиялык жолдор менен өндүрүлүшү мүмкүн.
20-кылымдын башында, аминокислоталар алгач синтетикалык синтез үчүн субстраттар катары колдонула башташты.ААлар негизинен фармацевтикалык жана косметикалык формулалардагы консерванттар катары колдонулат.Мындан тышкары, ААлар ар кандай ооруларга, шишиктерге, шишиктерди жана вирустарга каршы биологиялык жактан биологиялык жактан биологиялык жактан жигердүү деп табылды. 1988-ж Бүгүнкү күндө биотехнологияны өнүктүрүү менен, кээ бир аминокислоталар ачыткы тарабынан ири масштабда коммерциялык түрдө синтезделген, ал AAS өндүрүшүн экологиялык жактан көбүрөөк таза деп эсептейт.
01 Аминокислоталардын өнүгүшү
19-кылымдын башында, табигый түрдө пайда болгон аминокислоталар биринчи жолу ачылганда, алардын структуралары өтө баалуу деп болжолдонгон, амфипиляцияларды даярдоо үчүн чийки зат катары колдонсо болот. ААнын синтезинде биринчи изилдөө Бонди тарабынан 1909-жылы билдирди.
Ошол оку, Н-Экилгликин жана Н-Акылаланин сюрфактыктар үчүн гидрофильдик топ катары киргизилген. Андан кийинки жумуш Глинин жана Аланин жана Гентих жана Аланинди колдонуп Липоимино кислоталарынын (AAS) синтезине катышкан. Бир катар табылгаларды жарыялаган,Анын ичинде биринчи патенттик өтүнмө, үй чарбаларын тазалоочу азыктардын (мисалы, шампундар, жуугучтар жана тиш пасталары).Кийинчерээк, көптөгөн изилдөөчүлөр Ацил аминокислоталардын синтезин жана физикалык касиеттерин изилдеп чыгышты. Бүгүнкү күндө ААнын синтез, касиеттери, өнөр жай буюмдары жана биологиялык биологиялык ченемдеринде адабияттын ири органы жарыяланды.
02 Түзүмдүк касиеттери
ААнын аас кычкыл кычкылтек чынжырлары түзүлүшүндө, чынжырдын узундугу жана номери өзгөрүшү мүмкүн.ААнын структуралык ар түрдүүлүгү жана жогорку жер үстүндөгү композициялык ар түрдүүлүгүн жана физикалык жана биологиялык касиеттерин түшүндүрөт. ААнын башкы топтору аминокислоталардан же пепттерден турат. Башкы топтордогу айырмачылыктар бул беттик кишинин адисорбциясы, агрегаттоо жана биологиялык иш-аракеттерди аныктайт. Башталгы топтогу функционалдык топтор ААнын, анын ичинде Cationsic, Anion, ананционник жана амфотаричтин түрүн аныктайт. Гидрофильдик аминокислоталардын жана гидрофобиялык лонг-чынжырчанын бөлүктөрүнүн айкалышы, молекуланын жогорку бетин активдүү кылган амфипалык структурасын түзүшөт. Мындан тышкары, молекуладагы асимметриялык көмүртек атомдорунун болушу хирал молекулаларын түзүүгө жардам берет.
03 Химиялык курамы
Бардык пептиддер жана полипептиддердин дээрлик 20 α протеиногендик α-аминокислоталардын полимериизациялык буюмдары. Бардык 20 α-аминокислоталар карбоксил кислоталык функционалдык тобу бар (-cooh) жана аминокердик-функционалдык топ бар (2 -NH 2), экөө тең бирдей типробедралдык атомго бекитилген. Аминокислоталар бири-биринен α-көмүртекке тиркелген ар башкача айтканда (R тобун суутекти кошпогондо, ар кандай r) менен айырмаланат. Бул айырмачылыктар сууга чалдыккан аминокислоталардын эригүүсүн да аныктайт.
Аминокислоталар - бул гирал (глининден башка), алфа көмүртек менен төрт башка алмаштыруучусу бар, анткени алфикалык жактан активдүү активдүү. Аминокислоталардын эки мүмкүн болгон эки көрсөткүчү бар; Алар бири-биринин стереузомерлеринин саны бир кыйла жогору экендигине карабастан, бири-биринин күзгүсү эмес, бири-биринин күзгү эмес. Айрым аминокислоталарда (фенилаланин, Тиросин жана Триптофан) R-Group (фенилаланин, Тиросин жана Триптофан) эң көп дегенде 280 нм AIDIC α-KOUCH ЖАНА АМИНЦИЯЛЫК АМНАСЫНДАГЫ АМНА КОМИНОСИЗИЯЛАРЫ ИОНИКАЛЫКТАРДАГЫ ИОНЦИЯЛЫКТАРГА ЖАНА ЭРЕГИЗДЕРГЕ ЖАНА ЭРЕГИМДЕРИ ЖАНА ЭРКЕНИМИМДЕРИ ЖӨНҮНДӨГҮЛӨРДҮ КОЛДОЙТ, "Төмөндө иондоштуруу тең салмактуулугун куруу.
R-Couh ↔r-COO-+ H+
R-NH3+↔r-nh2+ H+
Жогоруда айтылгандай, иондоштуруу тең салмактуулугунда көрсөтүлгөндөй, аминокислоталардын кеминде эки алсыз кислоталык топтор бар; Бирок, карбоксил тобу аминокамдар тобуна салыштырмалуу бир кыйла кычкылдануу. PH 7.4, карбоксил тобу, аминока тобу прототолонат. Ионизаторсуз рОБулдары бар аминокислоталар бул документте электрдик бейтараптык жана zwitterion түзүлөт.
04 Классификация
ААлар төрт критерийге ылайык классификацияланса болот, анда төмөндө келтирилген кезек менен сүрөттөлгөн.
4.1 Келүү боюнча
| АРА боюнча ААларга 2 категорияга бөлүнсө болот. ① табигый категория Аминокислоталарды камтыган кээ бир табигый жол менен пайда болгон кошулмалар бетин / интерфикациялык чыңалууну азайтуу мүмкүнчүлүгүнө ээ жана кээ бирлери гликолипиддердин натыйжалуулугунан ашып кетишет. Бул аас ошондой эле липопепстид деп аталат. Липопепстиддер, адатта, бакиль түрлөрү тарабынан өндүрүлгөн молекулалык салмак кошулмалары.
Мындай аас андан ары 3 субклассаларга бөлүнөт:Сурфактин, итурин жана фенгицин.
|
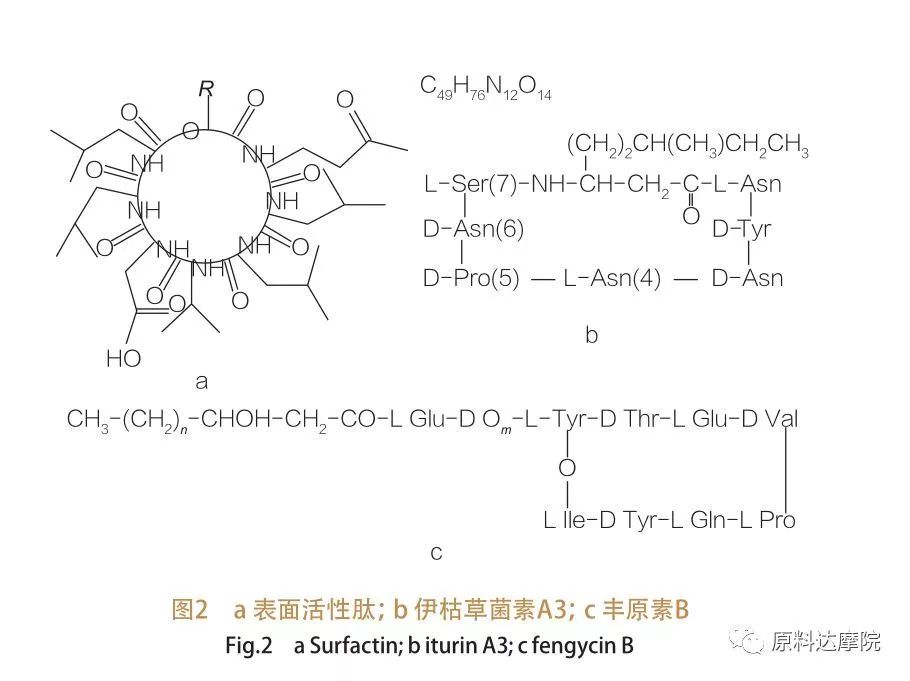
| Жер бетиндеги жигердүү пептиддердин үй-бүлөсү ар кандай заттардын гептипефтвидди курчап турат,2А сүрөтүндө көрсөтүлгөндөй, C12-C16 СЭСти сакталган β-гидрокси кычкылтек чынжыры пептид менен байланышкан. Беттик-жигердүү пептид - бул шыңгыроо β-гидрокси кислотасынын жана пептиддин ортосундагы C-терминалдын ортосундагы катализ аркылуу катализ аркылуу жабылган макрокикалык лактон. Итуринди субкласта, алты негизги варианттар, атап айтканда Итурин А жана С, Микосубтилин жана Бабышомицин Д, Ф жана Л.Бардык учурларда, гептафептиддер C14-C17 Amino семиз кислоталарынын CHITES (чынжырлар ар түрдүү болушу мүмкүн). Экзимиктер болгон учурда, β--позициядагы аминология тобу C-терминд менен биригиши мүмкүн
Субкласс фенкетинин курамында Фенгицин А жана В жана В, ал эми Трайтатин деп аталат.Декапэтидди C14 -C18 каныккан же бейкапар β-гидрокси кычкыл чынжырына байланыштуу. Пепстийдин ырааттуулугунун 3-позициясы 3-позициясы бар жана с-терминалдык калдыктар менен термелип турган пепастатин жана с-терминалдык калдыктар менен с-терминалдык калдык менен этардын калдыктары бар лактон болуп саналат.
② Синтетикалык категория AAS кислоталык, негизги жана нейтралдуу аминокислоталардын бирин колдонуп, синтезделиши мүмкүн. ААнын синтежиссисинде колдонулган жалпы аминокислоталар - бул глутамиялык кислоталык, серин, пролина, аспартикалык кислоталык кислотасы, Глицин, Аргинин, Аланин, Лейцин жана Белок Гидролизаттары. Бийликтин бул субклассы химиялык, ферментативдик жана химечиялык ыкмалар менен даярдашы мүмкүн; Бирок аас өндүрүү үчүн химиялык синтез экономикалык жактан мүмкүн. Н-люйл-л-глутамиялык кислоталык жана n-пальмиайл-л-глутамиялык кислотасы кирет.
|
4.2 Aliphatic Chain жибигеттерине негизделген
Алифатикалык чынжыр алмаштыргандардын негизинде аминокислотанын негизинде 2 түргө бөлүнсө болот.
Ээлеген кызмат орду боюнча
| ①n-Заменен N-алмаштырылган кошулмада, аминомопия тобу липофилиялык топ же карбоксил тобу менен алмаштырылат, натыйжада аксакалдардын жоголушуна алып келет. N-алмаштыруунун эң жөнөкөй мисалы - анил аминокислоталар, бул анил аминокислоталар, бул анил аминокислоталар. N-алмаштырылган ААнын гидрофобиялык жана гидрофилиялык бөлүктөрдүн ортосунда чоң байланыш бар. Амидеги облигация мүмкүнчүлүгүнө ээ, бул биологиялык курчап турган сыгылган суутеканын деградациясына көмөктөшөт.
②C-Заменен C-зомбулук кошулмаларында, борозлук тобунун ордун толтурат (AMIDE же ЭСТЕРДИН БОНГИЯСЫ). Типтүү с-заментсиз кошулмалар (мисалы, Эстер же Амиддер) - бул Cation Cationents.
③n- жана c-s-stament aas Амино жана карбоксил топтору бул түрүндө тең гидрофильдик бөлүгү болуп саналат. Бул түрү - бул амфотерикалык сюрфактан. |
4.3 Гидофобдук куйруктарынын саны боюнча
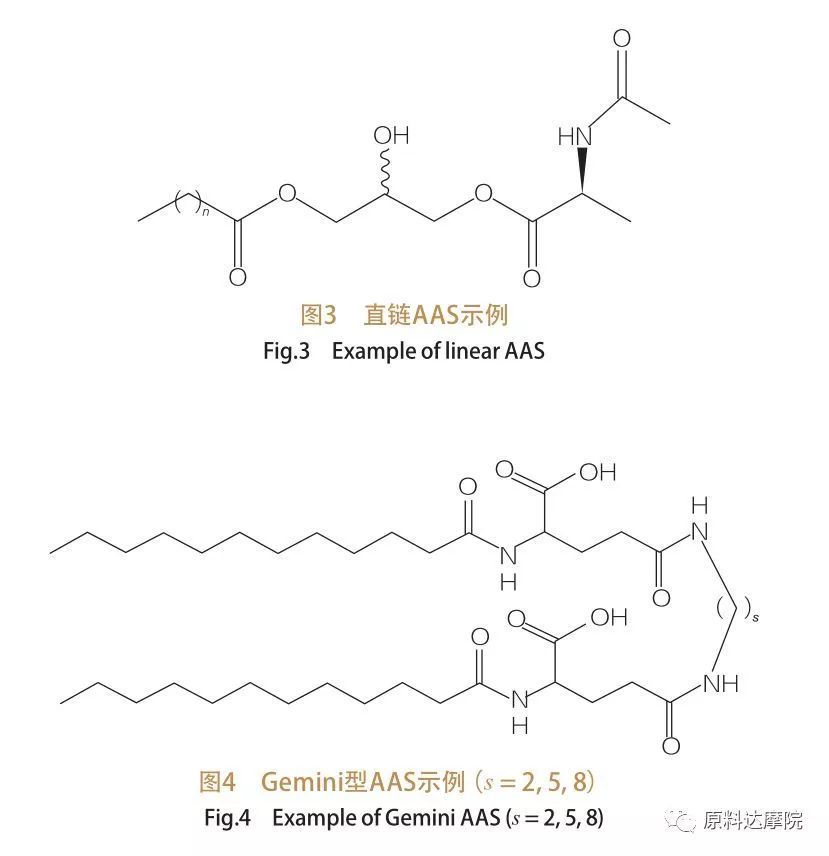
Башкы топтордун жана гидрофобиялык куйруктарынын санынын негизинде AAS төрт топко бөлүнүшү мүмкүн. Аас, Эгиздер (Димер) Тип AAS, GLYCEROLIPID түрү AAS, жана Bichephalic Asphiphilic (BOLA) AAS. Түз-чынжырчачылар бир гана гидрофобдук куйругу бар аминокислоталардан турган үстүңкү беттер (3-сүрөт). Эгиздер тиби AAS эки аминокислоталык полярдык калдыктар жана эки молекулага эки гидрофобдук куйруктары бар (4-сүрөт). Бул түзүлүштүн ушул түрүндө, эки түз чынжыр аас космостук менен байланышкан жана демек, димдер деп да аталат. Экинчи жагынан, Гликлолипиддин типтеги AASинде, ошол эле амин кислоталык башкы тобуна эки гидрофобиялык куйруктар тиркелет. Бул ботторлордун аногледиддеринин, дилликриддердин жана фосфолипиддердин аногладаттарына, фосфолипиддердин англиялары катары каралышы мүмкүн, ал эми Бола типтеги ААдагы AAS, Amino кислоталык башкы топтору гидрофобдук куйрук менен байланышкан.
4.4 Жетек-топ түрүнө жараша
①cationic AAS
Бөлүндүн ушул түрүнүн башкы тобу оң зарядга ээ. Эң алгачкы Cationedic AAS Этил Кокойл аргатинаты, бул пиррульдинан карбокдилаты. Бул сүттүн уникалдуу жана ар түрдүү касиеттери аны дедомент, антитробдук агенттерге, антистатат агенттерине, антистататтуу агенттер, чач кондиционерлерине, ошондой эле көзгө жана териге жана биологиялык жактан жумшак деп айтууга болот. Сингаре жана Махаб синтезделген аргинин жайгашкан Cationic Aas синтезин синтезделген жана физикахемалык касиеттерин баалады. Бул изилдөөдө алар схоттен-Бауман реакциясынын шарттарын колдонуу менен алынган продукциянын жогорку түшүмүн билдиришти. Алкыллдын чынжырынын узактыгы жана гидрофобустуулугун жогорулатуу менен, болжолдуу схеманын бетинин үстүнкү иши көбөйүү жана микробдун концентрациясы (ЖМБ) баса белгилөө үчүн (ЖМБ) баса белгиленди. Дагы бирөөсү - чачтын камкордугундагы шарттарда кондиционер катары колдонулган тикенектин сарамжалсыз кошулган протени.
②anionic Aas
Аноникалык сюрфактикада сюрпактандын полярдык башкы тобу терс зарядга ээ. Саркосин (CH 3 -NH-CH 2 -NOH, N-Methylgycine), деңиздеги деңиздеги жылдыздар менен жайгашкан аминокислота Глинингине (NH 2 -ч 2 -Cooh, 2 -Cooh,) химиялык жактан химиялык жактан жетиштүү. -Коо,) Сүт эмүүчүлөрдүн клеткаларында табылган негизги аминокислота болгон Глининге байланыштуу химиялык жактан байланышкан. Лаурдык кислотасы, тетраденоик кислотасы, олеиалдык кислотасы жана алардын шамы жана эс-кемы саркозинатты синтездөө үчүн колдонулат. Саркосинаттар акырындык менен, көбүнчө, шампундар, шампундар, чачырак куурулган көбүк, күндүзгү, теринин, тери тазалоо жана башка косметикалык өнүмдөрдө колдонулат.
Башка коммерциялык жол менен Аноникалык Аас • Натрий Н-Кокойл-Л-Глутамат жана Потасий Н-Кокойль Глутати үчүн фирмалык аталыштар, тиешелүү амилитегк-12, тиешелүүлүгүнө жараша. Амилит көбүнчө көбүк, эритүүчү, солубилизатор катары колдонулат жана шампундар, ванна самындар, денени жууп, тиш пасталары, тазалоочу самолёттор, байланыш линза тазалагычлар, баяндама Амисофт, негизинен, жоолук жана чачтарды тазалоо, негизинен, синтетикалык каражаттарды, дене камтыган буюмдар, шампундар жана башка теринин башка буюмдарын бөгөттөөчү, синтетикалык жуугучтуу жолдор менен тосуп алуу.
③zwitewersic же амфотерикалык аас
Амфотерикалык сюрфактниктер кислоталык жана негизги сайттарды камтыйт жана ошондуктан алардын PH наркын өзгөртүү менен алардын заряды өзгөртө алат. Алькалардын маалымат каражаттарында алар аниникалык сюрпайкчылыктарда болушат, ал эми кычкыл айлана-чөйрөлөрдө, алар кычкыл айлана-чөйрөдө жана ампфотерикалык сюрфактика сыяктуу бейтараптуулуктарга окшоп кетишет. Лурил Лизин (LL) жана Алкокси (2-Гидроектордук) Аргинин аминокислоталардын негизинде белгилүү ампфотар сюрфактери. Ll - лизин жана лаурик кислотасынын конденсациясы өнүмү. Анын амфотариалдык структурасына байланыштуу, айкалыштырылган жана кислоталык эриткичтерди кошпогондо, эритилгендиктин дээрлик бардык түрлөрү менен эрийт. Органикалык порошок катары гидрофильдик беттерге жана сүрүлүү коэффициенти менен сүрүлүү коэффициентине ээ, бул бүтүн сүрүлүүчү майлоочу жөндөмдү берүү мүмкүнчүлүгүн берет. Ll тери кремдеринде жана чач кондиционерлеринде кеңири колдонулат, ошондой эле майлоочу жай катары колдонулат.
④nonionic aas
Түлкүлөргө толгон-токой калкыраак топтор менен формалдуу айыптоолорсуз мүнөздөлөт. Сабаг ж.б. тарабынан жасалган сегиз жаңы ыктымал болгон сегиз жаңы ыктымал болду. Мунай эриген α-аминокислоталар. Бул процессте Л-Пенылаланин (Леп) жана Л-Лейцин алгач он алтылык менен, андан кийин пальмитикалык кислотасы менен бир-биринин аминокислоталардан эки эседен жана эки эседен кислотасы менен биримдикте болгон. Андан кумурскалар жана эс-селептер этилен кычкылы менен кычкылтек менен, үч ферниланин туундусун даярдоо үчүн үч феныланин дүнөттөрүн даярдайт (40, 60 жана 100). Булар акылсыз аасык жана көбүк касиеттери бар экени аныкталды.
05 синтез
5.1 Негизги синтетикалык маршрут
ААларда гидрофобдук топтордун амин кунчу кислотасына же аминокислоталардын каптал чынжырларына тиркелиши мүмкүн. 5-сүрөттө көрсөтүлгөндөй, ушул, ушул, төрт негизги синтетикалык маршруттар бар.
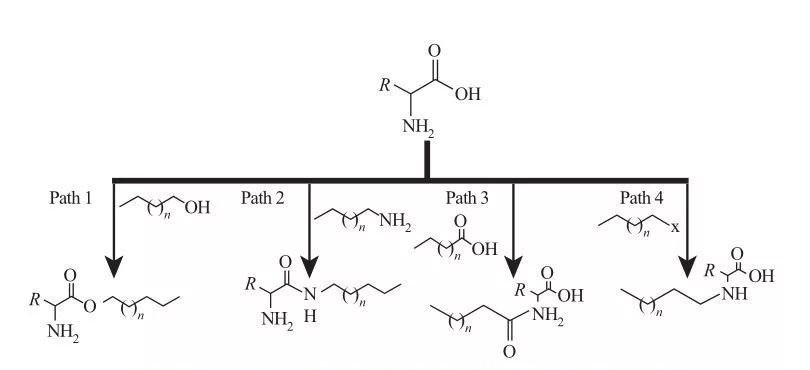
Аминокислота негизделген аминокислотанын беттешинин фундаменталдык синтези
| 1. Ампишилиялык эфирдик Эстер Аминдернигника реакциясы менен өндүрүлөт, бул учурда, синтездин синтези, адатта, семирткичтер жана аминокислоталар жана аминокислоталар менен жетишилген. Айрым реакцияларда, сульфурикалык кислота катализатор жана суусуздануучу агент катары иштейт.
PATHY 2. Амино кислоталары аминокислоталар менен актинокиндер менен реакцияга кабылышат, натыйжада амфийхилиялык амидаминдердин синтезине алып келет.
3. Амидо кислоталары Амидо кислоталары менен аминокислоталардын аминокислоталарынын топторун реакциялоо менен синтезделет.
4. Галоалкандар менен Амин топторунун реакциясы менен Лонг-чынжырлуу алькил аминокислоталар синтезделди. |
5.2 Синтез жана өндүрүштөги аванс
5.2.1 Жалгыз чынжырчанын синтези
Н-Экил же о-акыл аминокислоталар же пептиддер амин кислоталары бар Амин кислоталары бар амин кислоталары менен фермент-катализделген акитасы менен синтезделиши мүмкүн. Аминокислота Амиддин же Метил Эстердин туунду синтетези жөнүндө эң алгачкы отчет - Кандар Антарктида, Максаттуу аминокислотасына жараша 25% дан 90% га чейин түшүмдүү. Метил этил куметон ошондой эле кандайдыр бир реакцияларда эриткич катары колдонулган. Ойдонбанген ж.б. Ошондой эле липаза жана протеците-катализделген N-акчылыгы аминокислоталардын, белок гидролизаторлорунун жана / же органикалык эриткичтердин аралашмасын (мисалы, диметилформамид / суу) жана метилдин бутыл кумун менен (мисалы, димфетилформамид / суу) менен колдонгонун сүрөттөйт.
Эрте күндөрдө ААнын фермент-катализдин синтезинин негизги көйгөйү төмөн түшүмдүү болгон. Valivety et al. Н-тетраданоил аминокислотанын түшүмдүүлүгү ар кандай белгини колдонуп, бир нече күн бою 70 ° Cда инкубаторлордун түшүмү болгону 2% гана болгон. Montet et al. Майлуу кислоталар жана өсүмдүк майларын колдонуп, Н-Кычкылдын синтезиндеги аминокислоталардын түшүмдүүлүгүнө байланыштуу көйгөйлөргө туш болгон. Алардын айтымында, продукттун максималдуу кирешелүүлүгү узак мөөнөттүү шарттарда 19% болгон жана органикалык эриткичтерди колдонуу. Ушундай эле көйгөйдү Валиветти жана башкалар менен жолуктурган. N-CBZ-L-L-Lyzine же N-CBZ-Lysine метил эстеринин туундулары.
Бул изилдөөдө алар N-Кордолгон серинди субстанцат катары колдонууда 3-o-tetradecanoyl-л-Serine кирешелүүлүк 80% дешти. Липазаны, Л-Хомосерин, Л-Гомососин, Липазия Липосес жана Л-Корлес (Липаза) липаза (Липаза) липазанын сулуулугу менен липазалык л-хомосериндин жана л-серин алгандыгы бир аз төмөн болгонун кабарлаган жок Л-коркунучтуу аклатасы жана жолугат.
Көпчүлүк изилдөөчүлөрдүн арзан жана даярдалган аас синтезин синтезинин синтезин үчүн колдонууну колдошту. Soo et al. Пальма майына негизделген беттерди даярдоо гибобексиз липоензим менен мыкты иштейт деп ырастады. Алар белгилегендей, өнүмдөрдүн кирешелүүлүгү - реакцияны талап кылганына карабастан, алда канча жакшы болот. Герова жана Ал. Метонинин, Пролин, Лейцин, Шеннолин, Лейцин, Шенниланин жана фенилгинин, циклдүү / жарлык аралашмага негизделген синтездик жана беттик иш-аракеттерин иликтеген. Панг жана Чу аминокислоткананын синтезин жана дикарбоксил кислотасынын синтезин синтезин сүрөттөгөн синтезин, бир катар функционалдык жана биодридрдик аминокисттик-кислотасынын синтештирилишин синтезделегенин сүрөттөгөн.
Кантаэзене жана Геррейро Бок-Ала-О жана Бок-Асп-Оо, Лонг-Чаин Алифатикалык алкоголору менен Дихлороман менен, 4b (4b Сепероза 4b) катары Dichloromethane менен. Бул изилдөөдө Бок-Ала-Оо, 16 карбондордун майлуу алкоголору менен реакция жакшы түшүмдүүлүккө ээ болгон (51%), ал эми Бок-Асп-Ох 6 жана 12 слушасы бар, ал эми тиешелүү түшүмдүүлүк 63% [64]. 58% дан 76% дан 76% га чейин синтездештирилген, ал эми ар кандай узакка созулган облигациялар менен синтезделген CBZ-ARG-OME тарабынан жасалган майлуу жана семиз облигациялар менен синтезделген.
5.2.2 Эгиздер жайгашкан аминиялык аминокислота / Пептиддердин синтези
Аминокислота гееминге негизделген Эгиниялык схферкуляторлор эки түз чынжыр чынжыр аас молекуласынан туруштук бере алышат. Геминининин аминиялык аминокислоталык бюллетенинин (6 жана 7-сүрөттөр) 4 могензизм синтезинин 2 схемасы бар (6 жана 7). 6, 2-сүрөттө, аминокислота туундулары кошулма менен кошо космостук топ катары реакцияланат, андан кийин 2 гидрофобдук топ киргизилген. 7-сүрөттө, 2 түз чынжырчанын структурасы түздөн-түз бюфунцекталдык мейкиндиктеги топ тарабынан бириктирилген.
Геминдик липоимино кислоталарынын фермент-катализдин синтезин алгачкы өнүгүүсү Valivety жана al. Yoshimura et al. Цистин жана Н-Алкыл Бромайдга негизделген аминокислокке негизделген GEMINI-SURFAGTANT синтезин, адисорупция жана синморттук жана агрегат жүргүзүү. Синтезделген схфактенттер тиешелүү мономердик беттиктерге салыштырмалуу. Faustino et al. Л-Цистин, Д-Цистин, Д.-Цистин, Л-Цстюлин, Л-Цстеин, Л-Метинин жана алардын жуптары Эгиздеринин жуптары, алардын тең салмактуулугу боюнча жуптар Мономика менен Эгиздерди салыштырып, Джемериянын Мономерлеринин мааниси төмөн болгон деп көрсөтүлдү.
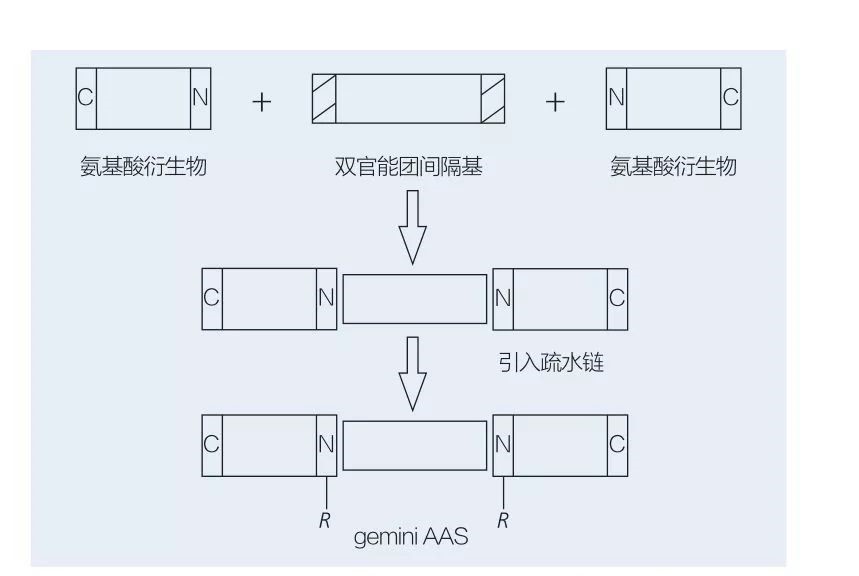
АА туундуларын жана космосторду колдонуп, GELEDSITION AAS синтези, андан кийин гидрофобдук топтун кыстаруусу менен
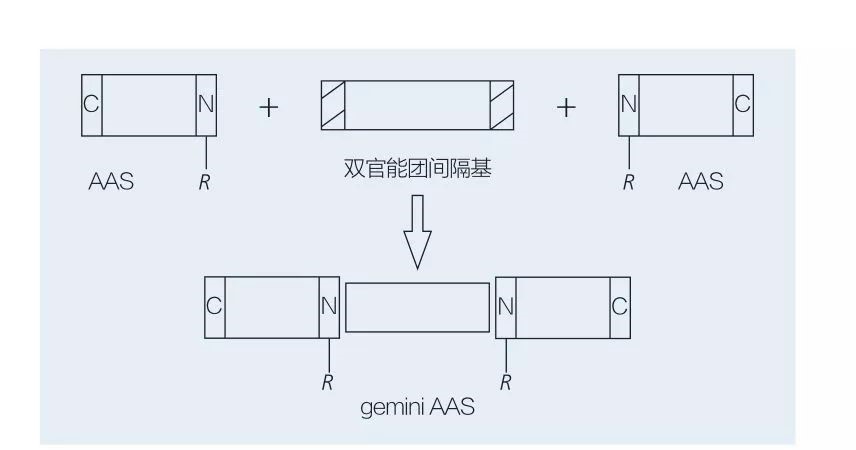
Gemini asass of Gemini asass of Bufunctional Spacer жана AASун колдонуп
5.2.3 Glycerolipid аминокислотанын синтези / Peptide Surfactles
Гликеролипид Амино кислотасы / Пепиддердин сюролору (же ди-) Эсторлордун жана фосфолиптердин структуралык аналогу, алардын бир-эки мүйүздүүлүгүнүн структуралык аналоги, бир-эки аминокислота чынжырларына байланыштуу структуралык аналогдук жана фосфолиптердин структуралык аналогу, эфирдик байланыштардын структуралык аналогу. Бул синтезин синтездик синтезинин бийик температурасында жана кислоталык катализатордун катышуусунда Глицер Минцол Эстирлеринин Эсторлорун даярдоодон башталат (мисалы, BF 3). Ферменттин катализдеген синтези (гидроласаларды, протекторлорду жана белгини колдонот) да катализатор катары колдонулат (8-сүрөт).
Папиндин жардамы менен папенди колдонуп, аргинин глинингесинин ферментиме синтезези билдирилди. Диасилглицер этаттын синтезчилери ацетыларгининден синтезд жана алардын физикахимиялык касиеттерин баалоодо дагы бааланган.
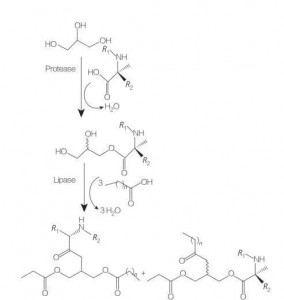
Mono жана DiaCylGlyColor аминокислотанын синтези
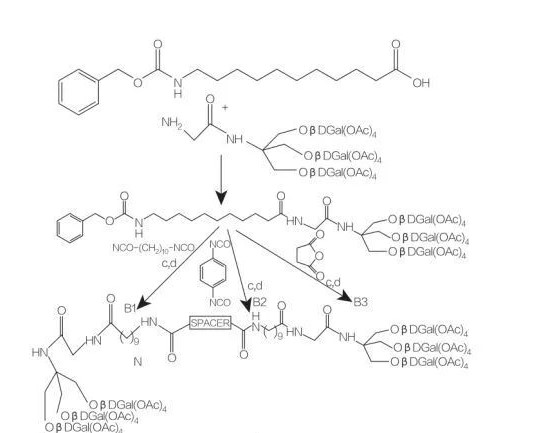
Spacer: NH- (CH2)10-Nh: Compoundb1
Spacer: NH-C6H4-Nh: Compoundb2
Spacer: ch2-Ч2: Compoundb3
Трис (Гидроксимил) Аминометриядан алынган симметриялыктардын синтези
5.2.4 Бола-амино кислотасынын / Пептиддердин синтези
Амино кислотанын негизиндеги Бола тибиндеги аминокислит бар 2 аминокислота бар, ал ошол гидрофобдук чынжыр менен байланышкан. Franceschi et al. 2 аминокислота (д- же л-аланин же л-хистидин) жана 1 Алкилдин ар кандай узундуктагы 1 Алкил чынжырынын синтезин синтезин сүрөттөгөн. Алар синфильмдин роман синтезин жана агрегатынын синтезин жана агрегатын аминокислота менен бөлүштүрүүнү талкуулашты Колдонулган аминокислоталар, Азидотиммин (AZIT) (AZT) сергек аминоаоид болушу мүмкүн (AZT) - АЗНБРЕНДЕГИ АМИНО Кулак, Норборн Амино кислотасы, аминокрогунун AZT алкоголунан алынган аминокколог (9-сүрөт). Трис (Гидометроксил) Аминометан (TRIS) менен алынган симметриялуу бола-тибиндеги синтез.
06 Физикоимдик касиеттери
Аминокислота негизиндеги схема (AA) ар түрдүү жана ар тараптуу мүнөздүү экендиги белгилүү жана жакшы эритмелер, эмульсиялуу касиеттери, жогорку натыйжалуулук, жогорку сарайдын жогорку натыйжалуулугу жана катуу сууга болгон жакшы каршылык көрсөтүлүшү белгилүү болгону белгилүү.
Аминокислоталардын (мисалы, жер үстүндөгү чыңалуунун) семестринин (ЖМБ, фазалык жүрүм-турум жана KRAFFF температурасы)
6.1 Микиши критикалык концентрация (ЖМБ)
Микелердин концентрациясы - бул биофильмдер менен өз ара аракеттенүү жана анын биофильмдер менен өз ара аракеттенүүсү сыяктуу эле, биодордук-үндөгөн жигердүү касиеттердин бири (гидрофобияны көбөйтүү), бомфтин наркынын калыңдыкунун төмөндөшүнө алып келет. Аминокислоталга негизделген схфактенттер кадимки сюрфактыктарга салыштырмалуу ЖМБ маанилерин төмөндөтөт.
Башкы топтордун жана гидрофобиялык куйруктардын ар кандай айкалыштары аркылуу үч аргинин жайгашкан AAS синтезделген аасын синтезделген жана ЖМБны жана ЖМБнын үстүндөгү чыңалууну (ЖМБнын чыңалуулары), ЖМБнын гидрофобдук куйругун жогорулатуу менен азайып баратканын көрсөтүп, алардын ЖМБны (ЖМБнын чыңалуулары) окушту. Дагы бир изилдөөдө, Сингре жана Махабдар N-α-Acyrarginine Surfactys CM-ЖМБ гидрофобиялык көмүртек атомдорунун (1-таблица) чейин төмөндөгөнүн байкады.
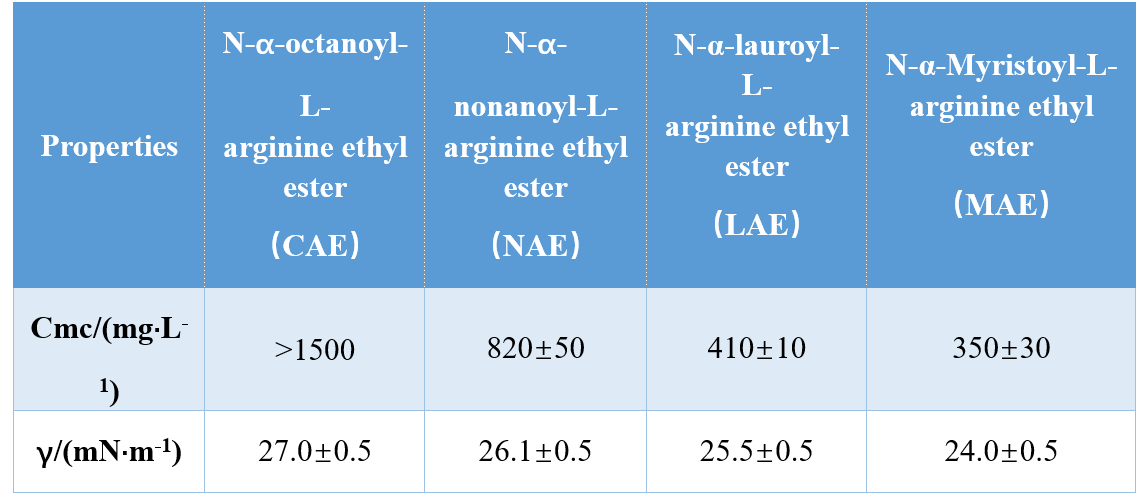
Yoshimura et al. ЖМБиндик жайгашкан ЖМБнын ЖМБны иликтеген ЖМБны иликтеген ЖМБнын гидрофобдук чынжырчасында көмүртек чынжырынын узундугу 10дон 12ге чейин жогорулаган ЖМБнын жогорулашына алып келген учурда, ЖМБнын көбөйүшүн андан ары көбөйттү, ал ЖМБнын агрегатынын төмөндөө тенденциясы төмөн экендигин тастыктады.
Faustino et al. кыстыкта жайгашкан Аноникалык Геминри Дирфорттенттеринин суу эритмелеринде аралаш микроэлектрдин калыптанышы жөнүндө билдиришти. Эгиздер боюнча схемактенттер тиешелүү кадимки моностериалдык беттер (C 8 CYS) менен салыштырылды. Липид-беттик аралашмалардын баалуулуктары таза сюрфактыктарга караганда төмөн болгон деп билдирилген. Эгиздер беттеги жана 1,2-дехептан "-сн-Глицерил-3-фосфоллин, суу эриген, суунун эритүүчү, микроэлль формофолипид, Миллимолердик деңгээлдеги ЖМБны түзгөн.
Шрестна менен Арамаки курт сыяктуу курт сыяктуу курт сыяктуу, аминикалык кислоталык анидиялык анондуктивдүү анондуктивдүү анондуктивдүү анидалык эмес, туздар болбогондо, илешкелик курт мээлеринин пайда болушун иликтеген. Бул изилдөөдө N-Dodecyl глутаматында KRAFFT температурасы жогору болгон деп табылды; Бирок, негизги аминокислота л-лысин менен нейтралдаштырылганда, ал микробдорду түзүп, эритмеси 25 ° Cде жаңыдан жаңы суюктук сыяктуу жүрө баштады.
6.2 Суу эриги
ААнын жакшы саздуусу кошумча ко-nh байланыштары бар экендигине байланыштуу. Бул AASди биологиялык жактан камсыз кылуу жана экологиялык жактан ылайыктуу шарттарга караганда көбүрөөк боорукер кылат. Н-акыл-л-глютамиялык кислотасынын суунун суусу, анын 2 карбоксил топторунун эсебинен да жакшы. CN (CA) 2 суунун суусу жакшы, анткени 1 молекуланын 2 иондук аргинин топтору бар, ал эми клетканын интерфейсинин жана андан да натыйжалуу бактериялык материалдык жактан айырмаланып, андан да натыйжалуу бактериялык тоскоолдуктарга диффузияга алып келет.
6.3 Krafft температурасы жана Krafft чекити
Крофт температурасы белгилүү бир температурадан ашып калган сюрпритациялык жумшак жүрүм-турумдун жүрүм-туруму катары түшүнсө болот. Иондук сюрфактуулардын суудан чөкпөгөн катуу гидратенттерди жаратууга тенденциясы бар. Белгилүү бир температурада (KRAFFFT температурасы), адатта, сюрпрактенттин чыгышынын кескин жана үзгүлтүксүз жогорулашы байкалат. Иондук сюртын KRAFFT чекити - бул ЖМБдагы KRAFFFT температурасы.
Адатта, бул нускадагы мүнөзгө ээ, ошондой эле төмөнкүдөй түшүндүрмөлөрдү түшүндүрсө болот жана төмөнкүлөрдү түшүндүрүүгө болот: Крофт чекитине жеткенге чейин, назик температуранын жаралышы чектелген, ал жерде анын эригичтиги акырындык менен акырындык менен көбөйөт. Толук эришимди камсыз кылуу үчүн, krafft чекитинен жогору температурада бланформалык формулаларды даярдоо керек.
ААнын температурасы изилденип, кадимки синтетикалык свфактиктер менен салыштырмалуу аргымалдык ААнын эказынын температурасын иликтеп, синфалиянын концентрациясы 2-5 × 10-6 мол-л -1, андан кийинки микроэлль формасы (Ohta et al. Алты синтезделген) N-Hexadecanoy AAS ар кандай түрлөрү жана алардын KRAFFFтин температурасынын жана аминокислотанын калдыктарынын ортосундагы байланышты талкуулады.
Тескерисинче, Н-Хексеноканын температурасы Амино кислотасынын калдыктарын азайтуу (фенлераланин) өлчөмүн төмөндөтүп, сандыктын жылуулугу (жылуулук жана жылуулук жана фенлераланиндин коштоосунда) көлөмү (жылуулук көтөрүлүү). Алтын жана фениилаланин системаларында, DL өз ара аракеттенүүсү N-HexadeCanoyl Aas тузунун катуу түрүндөгү өз ара аракеттенүүсүнөн күчтүү деп жыйынтык чыгарылган.
Brito et al. Микрокаторияны колдонуп, крифтикалык аминокислотанын температурасынын үч катар температурасынын температурасын аныктап, йодиид иондун айланасындагы TRIFLOOCHETATETETIATE, KRAFFFT температурасынын жогорулашына (болжол менен 6 ° C чейин), 47 ° C чейин 53 ° ° C чейин көбөйгөн. КМШ-кош байланыштардын катышуусу жана узак чынжырчанын сериясында катуулуулугу бар, ал эми KRAFFT температурасынын бир кыйла төмөндөшүнө алып келген. N-Dodecyl глутаматында KRAFFT температурасы жогору экендигин билдирди. Бирок, негизги аминокислота менен нейтралдаштыруу Л-Лизиндин натыйжасында Ньютон суюктуктары 25 ° C новний суюктук сыяктуу жүрүм-туруму боюнча микронный калыптуулукту пайда кылды.
6.4 Беттик чыңалуу
Беттик чыңалуулары гидрофобдук бөлүктүн чынжырынын жанына байланыштуу. Чжан и Ал. Вильельмиянын плитасынын методу (25 ±± 0,2) ° C (25 ± 0,2) ° C, ЖМБнын 3 МН-М -1, ЖМБнын 3 МН-М -1, ЖМБнын үстүндөгү тирешүү наркы аныкталды. Yoshimura et al. 2C N Cys тибиндеги чыңалуудагы аминокислотанын бетиндеги беттик үстүндөгү чыңалуудагы чыңалуу, 2C N Cys-га негизделген беттик активдүү агенттердин чыңалуулары. ЖМБнын бетинин чыңалышы ЖМБнын чыңалышы чынжырдын узундугуна чейин төмөндөгөнүн аныкталды (N = 8), ал эми n = 12 же узунураак чынжырдын узундугу үчүн тенденция жокко чыгарылган.
Дикарбокилделген аминокислокке негизделген беттик беттик чыңалуудагы сорстун 1-бетинин таасири дагы изилденген. Бул изилдөөлөрдө 2-кутучада 2 дикарбендүү аминокислотанын типтеги схемаларынын схемаларына (C12 Мална 2, C12 ASPNA 2 жана C12 ГЛуна 2) ЖМБдан кийинки бөксө баянын баалуулуктары салыштырмалуу болгон, ал эми жер үстүндөгү тирешүү CAC1 2 концентрациясына чейин төмөндөгөнү аныкталды. Бул кальций иондордун газ суу интерфейсинин интерфейстин интерфейсти жайгаштыруу боюнча кальций иондорунун таасири менен байланыштуу. Н-Dodeclaminomalonomalonamalonate жана N-Dodecylaspartate туздарынын бети, экинчи жагынан, 10 мл-ммол-л -1 -1 CAC1 2 концентрациясына чейин дээрлик туруктуу болгон. 10 MMOL-L -1 жогору, жер үстүндөгү тирешүү, жаан-чачындын кальций тузунун жаан-чачындын пайда болушуна байланыштуу кескин көбөйөт. Н-Dodecyl Glutamate үчүн Н-Додизил глутаматынын Түзүлүшү үчүн, схеманын орточо толушунун бир кыйла төмөндөшүнө алып келген, ал эми 2 концентрацияга көбөйүүдөн кийин, 2 концентрациялануунун жогорулашына алып келген.
Газ-суу интерфейстин AAS адистордук кинетикасын аныктоо үчүн, Газ-суу интерфейстин интерфейстин AASин аныктоо үчүн, көбүк басымдын максималдуу ыкмасын колдонуу менен аныкталган. Натыйжалар эң узун сыноо убактысы үчүн, 2C 12 Cys динамикалык беттик тирешүү өзгөргөн жок. Динамикалык жер үстүндөгү чыңалуунун төмөндөшү концентрацияланууга, гидрофобиялык куйруктарынын узундугу жана гидрофобдук куйруктарынын санынан гана көз каранды. Бүтүндүктүн концентрациялануусун жогорулатуу, чынжырдын узактыгын азайтуу, ошондой эле чынжырлардын саны тездик менен бузулган. C n cys (n = 8 ден 12ден 12ге чейин) жогорку концентрациялангандыгы үчүн алынган натыйжалар Wilhelmy методу тарабынан өлчөнөт.
Дагы бир изилдөөдө, Натрий Дидеекаминанын динамикалык бети (SDLC) жана Натрий-Дидихаминанын цистининин динамикалык бети (SDLC) жана Натрий-Дидихаминанын цистины менен аныкталды. Жарыялаган облигациялардын реакциясы башка ыкмалар менен дагы бир жолу иликтенди. МеркаптоОтханолдун кошуусунун 0,1 млн. Naclo SDLCдин слълниялык кислоталык топторго бөлүнбөгөн облигацияларын кычкылдангандан бери, Naclo (5 MMOL-L -1) 0,1 MMOL-L -1 SDLC чечимине кошулганда, агрегаттар байкалган жок. Электрондук микроскопия жана динамикалык жарык жарыктандыруу жыйынтыктары көрсөткөндөй, чечимде эч кандай агрегаттар түзүлгөн эмес. SDLCтин үстүндөгү чыңалуусу 34 Мн-М -1ден 60 мл-мн-м - болжол менен 20 мүн.
6.5 экилик жердин өз ара аракеттери
Жашоо илимдеринде бир катар топтор Cationsic AAS (диасоликалык аргисердик аргинин) жана фосфолипиддердин жана фосфолипиддердин префолиптери, акыры идеалдуу эмес мүлк электростатикалык өз ара байланыштын жайылышына себеп болот деп жыйынтыктады.
6.6 Агрегаттоо касиеттери
Динамикалык жарык чачуу аминокислоткананын агрегаттоо касиеттерин жана ЖМБнын концентрациясында, гидродинамикалык диаметри DH (= = 2р з) дх (= = = 2р з) түзгөн. C n Cys жана 2CN тарабынан түзүлгөн агрегаттар салыштырмалуу чоң жана башка беттерге салыштырмалуу кеңири масштабдуу бөлүштүрүү бар. 2C 12 Cys эске албаганда, бардык беттиктер, адатта, болжол менен 10 нм түзөт. Эгиздер боюнча схемаларынын мицеллинин өлчөмдөрү алардын мономери боюнча кесиптештерине караганда кыйла чоң. Углеводороддун чынжырынын узундугунун көбөйүшү, микроэллдин көлөмүнүн көбөйүшүнө алып келет. Охта ж.б. Н-Додизил-феныль-Аланыл-Аланыл-Аланыл-Пеныль-Пеныль-Пеныль-Аланин Тетраметиламммонийинин үч башка стереузомомерлеринин стереозомулерлорун сыпаттап, диастероосерлердин суу эритмесинде бир эле катуу агрегаттык концентрацияга ээ экендигин көрсөттү. Iwahashi et al. Тегерек дихромизм, NMR жана буу буу басымы Осмометриясы Н-ДодеКаноил-Л-Глутамдык кислотасынын, N-DodEcamic кислотасынын ири агрегаттарынын түзүлүшү жана алардын метил эсиндеринин ар кандай эриткичтеринде (тетрахидрофуран, ачонитри жана 1,4-Диоксан жана 1,2-Дичлороатан) Ротациялык касиеттери тегерек дихромизм, NMR жана буу басымы осмометриясы иликтеген.
6.7 Interfacion Adsortion
Амино кислоталык сюрфактенттиктеринин интерфактикасы жана анын кадимки кесиптеши менен салыштыруу илимий кесиптеши менен салыштырганда изилдөө багыттарынын бири. Мисалы, жыпар жыттуу аминокислоталардын доцатикалык аминокислоталардын доцисттик стерлотердин доцисттик эфирлердин эс-тутумунун инсорциялык касиеттери иликтенди. Натыйжалар көрсөткөндөй, Lep гезити маектешүү интерфейсинин интерфейсинин жана суу / гександы интерфейсте, тиешелүүлүгүнө жараша сууну жана сууну / хексан интерфейсте жайгашкан.
Борс ж.б. Дикарбендүү аминокислота-сууну газдалган аминокислота сюрписасындагы чечимдерди иликтөө, Додисл Глутаматынын, Доцицал Аспартаты жана Аминомалон (3, 2 жана 1 көмүртек атомдорунун) Бул отчетто айтылгандай, Дикарбукилеленген беттик жымдары MonoCarbelled Dodecyl Glycine тузуна караганда 4-5 эсе жогору болгон. Бул Dicarboundallated борфордериңиз менен кошуна молекулалардын ортосунда диагонилдүү бөрт беттери менен коңшу молекулалардын ортосунда түзүлүш берилет.
6.8 фазалык жүрүм-турум
Изотроптикалык ырааттуу жасалгаланган кубт фазалары өтө жогорку концентрацияда байкалат. Чоң топтор менен өтө көп ири топтор бар молекулалар кичинекей позитивдүү ийриликтин агрегатын түзүшөт. Маркес ж.б. 12ld12 / 12SER жана 8ld8 / 16sh тутумун изилдеп, жыйынтыктоочу символдо 12ly8 / 16sherser Ellyser Earn тутуму 4 фазалуу чөлкөмдө өтүүнү көрсөттү (Чакан Микерландиянын фазасынын жана Везник фазасынын ортосундагы) аймак). 12LY12 / 12SER тутумунун VESCICLES аймагы үчүн, ар дайым микроэлль менен биргеликте микроэлль менен бирге жашоону бир жашыраак, ал эми 8лс8 / Эскердин Весикулдары гана бар.
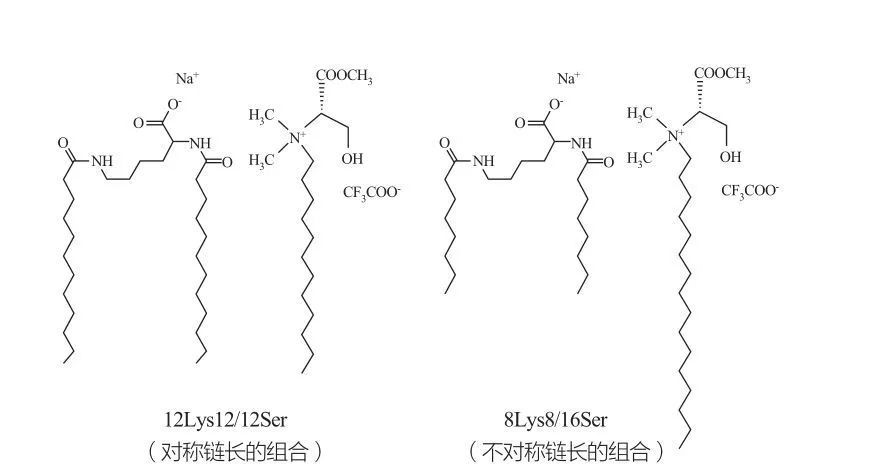
Лизиндик жана серинге негизделген катаникалык аралашмалар: Симметретриялык 12lls12 / 12sher (сол) жана асимметрия 8ly8 / 16sh up (оңдо)
6.9 Эмулсиялоо жөндөмү
Бачи ж.б. N- [3-Dodecyl-2-HydroxyPropy -l -l-arginine, l-glutamate and башка AA жана башка аас-тилдин эмиссиясын жана илешкектүүлүктү, интервьюзияны жана илешкектүүлүктү караган. Синтетикалык схфактилерге салыштырганда (алардын кадимки жана амфотикалык кесиптештери) менен салыштырганда, натыйжалары ААнын кадимки сюрфактуулдыктардан күчтүү жөндөмдүүлүгүнө ээ экендигин көрсөттү.
Baczko жана Al. Синтезделген роман анинциялык аминокислота беттери жана алардын жарактуулугун хиральга багытталган nmr спектроскопи эриткичиктери катары изилдеп чыгышты. Сульфонатка негизделген амфипхилиялык л-пге же л-ала туундулары ар кандай гидрофобдук куйруктары бар туундулар (Пентил ~ Тетрадцель), аминокислоталарды О-сульфензойдук ангидрид менен реакциялоо менен синтезделген. Wu et al. Н-майлуу ACYL AAS туздалган натрий туздары жанаНатыйжада мунай фазасына караганда мунай фазасына караганда мунай фазасына караганда мунай фазасына караганда мунай фазасына караганда бул беттиктер этил ацетациясы менен жакшыргандыгын көрсөттү.
6.10 Синтез жана өндүрүштө
Суу оор туруштук беттештер катуу суунун ичинде, б.а. кальций самыны менен жаан-чачын болбой турган жаан-чачынга каршы туруштук берүү жөндөмү деп түшүнсө болот. Суунун жогорку катуу каршылыгы бар суунун катуу каршылыгы бар дүүлүгүүсү жана жеке кам көрүү продуктулары үчүн абдан пайдалуу. Суу куршуулары кальций иондорунун катышуусунда өзгөрүүсүздүгүн жана жер үстүндөгү иш-аракеттердин өзгөрүшүн эсептөө менен бааланса болот.
Суу каршылыгын баалоонун дагы бир жолу - кальций самыны 100 г натрийден турган кальций самыны менен калыптанган кальций самыны үчүн пайыздык же граммды эсептөө саналат. Катуу суу, кальций жана магнез иондорунун жогорку концентрациялары бар аймактарда айрым практикалык колдонмолорду татаалдаштырса болот. Көбүнчө натрий иону синтетикалык аноникалык бюрпактандын каршы иону катары колдонулат. Бүткүл жер бөлүктөн турган жер үстүңөр беттик молекулаларга байланган болгондуктан, ал сюрпритантка жетишүүдөн көбүрөөк, андан аз болушу мүмкүн.
АААнын катуу каршылыгын изилдөө афицианттын жана катуу суунун каршылыгы кошумча карбоксил тобуна таасир эткендигин жана кислоталык жана суунун жана катуу сууну каршылык көрсөткөн эки карбоксил топторунун ортосундагы космостук топтун узундугунун жогорулашына алып келгенин көрсөттү. Кислотанын жана катуу суунун туруктуу каршылыгынын буйругу C 12 Глинат <C 12 Aspartate <C 12 глутамат. Диккарбокилделген Аминдлидди жана Дикарбоксилделген аминокавиттик амино бюрпактантын салыштыруу, тиешелүүлүгүнө жараша, экинчисинин ресинин кеңири жайылышы жана анын үстүнө кислотанын коштоосу менен көбөйгөнүн аныкталды. Диккарбомбатолдолгон N-Alkyl аминокислоталар кальций иондорунун катышуусунда соккон эффектин көрсөтүштү, жана с 12де ак гель түзүлгөн. 12 Глютамат жогорку CA 2+ концентрациясында жогорку беттик иш-аракеттерди көрсөттү жана деңиз суусунун десалисинде колдонулушу күтүлүүдө.
6.11 Дисперсия
Диссперссиздик бюрпакт билинбестен, сюрпрактенттин чөкмөлөрүн жана чөкмөлөрдүн чечимин чечүү мүмкүнчүлүгүн билдирет.Диссперссиздик - бул сюрфактыктардын маанилүү касиети, аларды пайдалангандардын, косметика жана фармацевтикада колдонууга жарактуу кылат.Дисперсиялык агент гидрофобдук тобу менен терминалдык гидрофилиялык тобунун (же түз чынжырчан гидрофобиялык топтордун арасында) эфирдик, эфир, үрөй учурарлык же аминок байланышта болушу керек.
Жалпысынан, алканоламидо сульфаттар жана ампфотарикалык сульфактаттар сыяктуу аноникалык сюрфактуулар, мисалы, көп кальций самын үчүн чачыранды агенттер катары колдонулат.
Көпчүлүк изилдөө жүргүзүү аракеттери ААнын аксталуулугун аныктады, ал жерде Н-Лайурыл Лайкс суу менен начар шайкеш келген жана косметикалык формулаларды колдонуу кыйынга турган.Бул серияда N-Acyl-Затын заманбап аминокислоталар боюнча, формулаларды өркүндөтүү үчүн косметикалык тармакта колдонулат.
07 уулуу
Кадимки сюрфактенттер, айрыкча Cation Cationents, суу организмдерине өтө уулуу. Алардын курч ылаңы менен клетка суу интерфейсинин үстүнөн адсорбцият-ион өз ара аракеттенүү феноменинен улам келип чыгат. Адатта, алардын үстүндө өзүлөрүнүн бийик уулуктуулугуна алып келген, адатта, алардын бийик уулуктарынын натыйжасында пайда болгон сюрфактыктардын күч-кубаттуу адистерине алып келет. Багыттардын гидрофобдук чынжырынын узундугунун көбөйүшү, ошондой эле үстөл курч уулуу уулунун көбөйүшүнө алып келет.Көпчүлүк ААнын көпчүлүгү, адамдар үчүн жана айлана-чөйрөгө (айрыкча деңиз организмдерине) аз же айлана-чөйрөгө (айрыкча деңиз организмдерине) азык-түлүк ингредиенттери, фармацевтика жана косметика катары колдонууга ылайыктуу.Көптөгөн изилдөөчүлөр аминокислота беттиктер жумшак жана териге кыжырданбашы керектигин көрсөттү. Аргининге негизделген бөртпактары кадимки кесиптештерине караганда уулуу болбошу керек.
Brito et al. Амино кислоталык амин кислотасынын физикалык жана токсикологиялык касиеттерин жана алардын туундулары (Tyr), гидроксипполин (Hyp), серин (сөө), стихиялуу безге (als) өзүнөн-өзү пайда болуп, алардын курч уулуу мүнөзү боюнча маалыматтарды берди. Алар доцидтриметиламфитиламмонийдин (DTAL) / Лиз-деривативдер жана / же сервивативдик аралашмаларды синтезделештиришкен жана алардын экотоклугу жана гемолитикалык потенциалын сынап көрүштү.
Rosa et al. ДНКнын туруктуу аминокислокке негизделген Cationedice VECICS-ге изилденген (ассоциация). Кадимки Cation Cationentiffacts айырмаланып тургандай, көп учурда уулуу болуп көрүнгөн, Cationsic Amino Acid-сюрфактенттеринин өз ара аракеттенүүсү уулуу эмес окшойт. Cation Cationent aas аргининге негизделген, ал өзүнөн-өзү туруктуу везикулаларды аниялыктар менен айкалыштырып, бир-бирден аниялыктар менен айкалыштырат. Амино кислотасынын негизинде датка ингибитендери уулуу эмес деп билдирилген. Бул беттиктер жогорку тазалыкты (99% га чейин), арзан баада, оңой биологиялык жактан, ал эми сууда толугу менен эрийт. Бир нече изилдөөлөр көрсөткөндөй, күкүрт аминокислота сюрфактери
Акыркы окууда Перинелли жана Ал. кадимки сюрчтанга салыштырганда рхматолипиддердин канааттандырарлык токсикологиялык профили билдирди. Рхамнолипиддер жетишсиздикти өркүндөтөт деп белгилүү. Ошондой эле алар Рухнолипиддердин эпителий баңгизатынын эпителийге берилишине таасирин билдиришти.
08 Antimicrobial иш
Сюрфактенттин антимдиклошуу иш-аракеттери минималдуу ингибитордук концентрация жолу менен баалана алат. Аргинин негиздеринин антитробдук иш-аракеттери деталдуу изилденет. GRAM-терс бактериялар GRAM-позитивдүү бактерияларга караганда, аргинин негиздерине барабар болгон деп табылды. Адатта, беттик аракеттердин антимдиклоштук иши, адатта, Аскыл чынжырларындагы гидроксил, циклопропан же ташталган байланыштардын болушу менен көбөйөт. Castillo et al. Аскыл чынжырларынын узундугу жана позитивдүү заряддын узактыгы молекуланын HLB наркынын (гидрофильдик липофилдик балансын) жана алардын мембраналарды бузуу жөндөмүнө таасир этет. Нё-Экылгинин Метил Эстери - бул кеңири спектрдеги антимдик иш-аракеттери бар Cationents сюрфактуулардын дагы бир маанилүү классы жана ал биологиялык биологиялык жактан жабылса жана төмөн же эч кандай уулануу жок. Нё-Акыларгинин метил эс-бетинин өз ара аракеттенүүсүндө 1,2 диплмитый-сн-Sn-Propytriox-3-Phoshorylcholine жана 1,2-дитетродекс-3-Propytrioxyl-3-Phoshorylcholine, модель кабыкчалары жана тирүү организмдер, бул тышкы тоскоолдуктардын жоктугу БУЛ СӨЗ САБАКТАРЫ БАКТЫЛЫКТАРДЫН АЛТИМБИАЛДЫКТИН НОМУМДАРЫ БАРЬФАЦТОРДОРДУН БАНКИБАКТАЛЫК ИШМЕРДҮҮЛҮГҮ БИЛИМДИ КОРГОЙТ.
09 Регеологиялык касиеттери
Бийликтин реологиялык касиеттери ар кандай тармактарда, анын ичинде тамак-аш, фармацевтика, мунайды казып алуу, жеке багуу жана үйдүн кам көрүү азыктарын аныктоодо жана алдын-ала ролду ойношот. Амино кислоталык бактылуулардын жана ЖМБнын илешкектүүлүгүнүн ортосундагы мамилелерди талкуулоо үчүн көптөгөн изилдөөлөр жүргүзүлдү.
Косметикалык өнөр жайда 10 өтүнмө
ААлар көптөгөн жеке кам көрүү өнүмдөрүн түзүүдө колдонулат.Потасий Н-Кокойл сызыгы териге жумшак деп табылат жана шлакты жана макияжын алып салуу үчүн жандыкты тазалоо үчүн колдонулат деп табылат. Н-Акыл-Л-Глутамиц кислотасы эки карбоксил топтору бар, бул аны сууну эрийт. Ушул ААнын арасында с 12 майлуу кислоталарынын негизинде CHETTIE кислоталарында кеңири колдонулат. AA C 18 чынжыры менен, териге кам көрүүдөгү эмульсиаторлор катары колдонулат, N-Lauryl Alanine Туздарынын туздары териге кыжырданбаган кремдүү көбүк жаратып, наристелердин камкордук азыктарынын формуласын түзүүдө колдонууга болот. Тиш пастадагы N-Lauryl компаниясында колдонулган аас самын жана күчтүү ферменттин натыйжалуулугуна окшош
Акыркы ондогон жылдар бою косметика, жеке кам көрүү продуктулары жана фармацевтика үчүн өзүлөрүн жана фармацевтика үчүн өз уулукка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка, жумшактыкка (жоошуна »басым жасады. Бул өнүмдөрдүн керектөөчүлөрү кыжырдануу, уулуу жана экологиялык факторлорду билишет.
Бүгүнкү күндө ААлар көптөгөн шампундарды, чачтын чочколорун жана мончо самынын түзүү үчүн колдонулат, алардын салттуу кесиптештеринин жана жеке кам көрүү продуктуларына көптөгөн артыкчылыктардан улам колдонулат.Протеинге негизделген беттер жеке кам көрүү үчүн зарыл болгон касиеттери бар. Айрым AAS тасмасынын мүмкүнчүлүктөрү бар, ал эми башкаларга көбүккө ээ болгон мүмкүнчүлүктөргө ээ.
Аминокислоталар табигый түрдө торунун торуна чейин нааразычылыгын туудурган маанилүү факторлор. Эпидермал клеткалары өлгөндө, алар стрратумдун курамына кирип, инстризиялык белоктор бара-бара аминокислоталарга деградацияланат. Андан кийин бул аминокислоталардын андан ары стратумга ташылып, семиз же семиз заттарды эпидермалдык стратумдун торуна салып, семиз заттарды сиңирип, теринин бетинин ийкемдүүлүгүн жогорулатуу. Теридеги табигый нааразалык фактордун болжол менен 50% аминокислоталардан жана пиррультенондон турат.
Коллаген, жалпы косметикалык ингредиент, ошондой эле теринин жумшак кармаган аминокислоталар бар.Тери көйгөйлөрү, мисалы, катуулук жана уялуулук сыяктуу, аминокислоталардын жоктугуна байланыштуу. Бир изилдөө көрсөткөндөй, аминокислотаны майлоочу жыпар жыттуу зат түтөтүп, жабыр тарткан аймактар кадимки абалына келбей, кадимки абалына кайтып келишкен.
Аминокислоталар бузулган кычыштырууга кам көрүүдө абдан пайдалуу деп табылды.Кургак, калыптабаган чачтар аминокислоталардын концентрациясынын кыскартылышынын төмөндөшүн белгилей кетиши мүмкүн. Аминокислоталар синфиктин чачын чачына кирип, териден ным сиңирүүгө мүмкүнчүлүк алышат.Аминокислотанын жайгашкан жосуну аларды шампундордо, чачтын жыргалчылыктары, чачтын жумшартуу, чач кондиционерлерине жана аминокислоталардын катышуусуна абдан пайдалуу кылат.
Күнүмдүк косметикада 11 арыз
Учурда амино кислоталык жол менен жуугучтук формулаларга болгон суроо-талап бар.ААларын тазалоо жөндөмүн, көбүктөнүүчү жөндөмдүүлүктү жана кездемелерди жумшартуучу касиетке ээ экендигин, аларды үй жумуштары, шампундар, денеге жуугучтарга жана башка колдонмолорго ылайыктуу кылат.ASPARCIC кислоталык туунду амфотерикалык аас касиет касиеттери менен жогорку натыйжалуу жуугуч болуп саналат. Тери дүүлүгүн азайтуу үчүн N-Алкыл-β-AminoThokxy кислоталарынан турган жуугуч ингредиенттерин колдонуу табылды. Н-Кокол-β-β-am-aminopropopropropиятынан турган суюктук жуугуч формулировкасы металл беттериндеги мунай тактары үчүн натыйжалуу жуугуч болгон деп билдирилген. AminoCarbound кислотасы схфактан, с 14-кофх 2 куна, текстиль, килемдерди, чач, айнекти ж.б.у.с.
N- (N'-Long-Chain Acyl-β-Аланлинге негизделген жуугучту даярдоо) Кейко менен Тацуянын жуунуусуна жана туруктуулугуна жана туруктуулугуна патенттин патентинде, оңой эле күрөк жана жакшы кездемелер менен алектенип келген. Као N-ACYL-1 -N-Gydroxy-β-Alanine компаниясынын негизинде жүйөлүү формуланы иштеп чыгып, териге кыжырдануу, суу каршылык, жогорку суу чаралуулары жана бийиктигин жоюу күч.
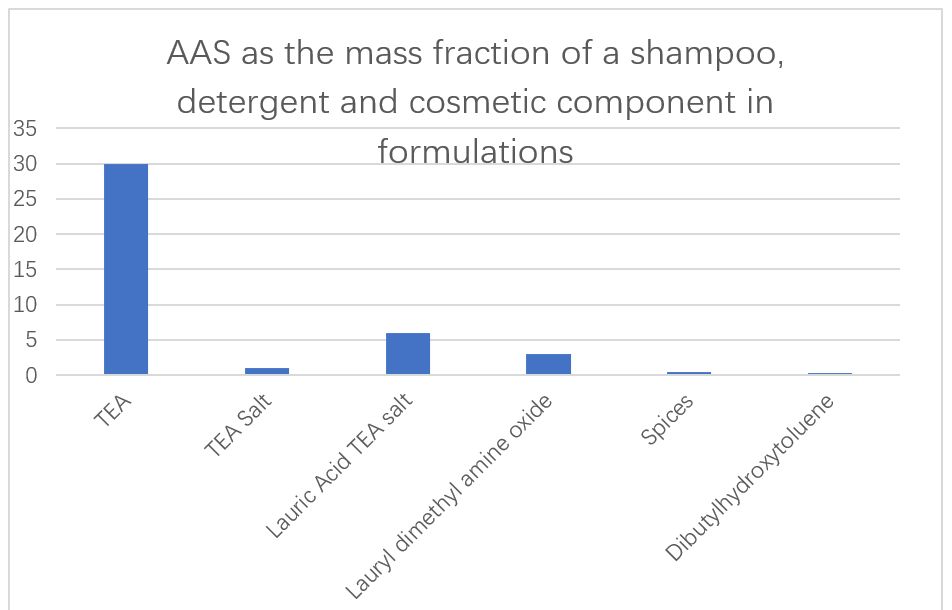
Ажиномото компаниясы Л-Глутамдык кислотасынын, Л-Аргининге жана Л-Лысинге негизделген аз уулуу жана оңой деградасыз дегледалуучу AAS колдонот (13-сүрөт). Белоктордун уятсыздыгын алып салуу үчүн ферменттин кошумчаларынын мүмкүнчүлүктөрү билдирилди. Н-Октамикалык кислотадан, Аланин, Метилгликинден, серин жана аспаркалык кислоталык суюктук каражаттары катары колдонулган суюктук чөлкөмдөр катары колдонулгандыгы үчүн алынган. Бул беттик адамдар илешкектүүлүктү жогорулатпайт, атүгүл өтө төмөн температурада да, бир тектүү көбүк алуу үчүн, көбүк шайманынын сактоочу жайларын оңой эле өткөрүүгө болот.
Пост убактысы: июнь-09-2022

